近日,深圳信立泰替格瑞洛片仿制药的上市申请已完成了技术审评工作,CFDA信息公示平台显示的办理状态变更为"在审批"。按照通常审批的时限来估算,CFDA将于本月底或下月初完成最后的审批工作,这预示着国产替格瑞洛片仿制药即将上市,信立泰近期有望拿下这款重磅药物的国内首仿。
攻破原研药物专利护城河为首仿上市铺平道路
替格瑞洛是阿斯利康开发的第一个可逆结合、直接起效、口服给药的新型P2Y12受体拮抗剂,这款药物于2011年7月获得FDA批准,2012年12月进入中国市场,商品名为"倍林达"。该药物属于抗凝血药,药理作用与氯吡格雷相近,临床主要用于心、脑血管血栓事件的预防和治疗,降低血栓性心血管事件的发生率。
从全球范围来看,抗凝血药一直都是各大制药企业竞相争夺的市场。在这一细分领域,阿司匹林是元老级的抗凝血药物,在临床中作为一级预防用药;1997年上市的氯吡格雷是阿司匹林之后的又一款重磅抗凝血药物,年销售额的峰值曾接近100亿美元。
作为氯吡格雷的换代品种,替格瑞洛不需要经过肝脏代谢激活,对于血小板的抑制作用更强、起效更为快速,能显著降低心血管死亡、心肌梗死或卒中的发生率,自上市以来已经被多部欧美治疗指南推荐为ASC患者的一线或首选抗血小板药物。
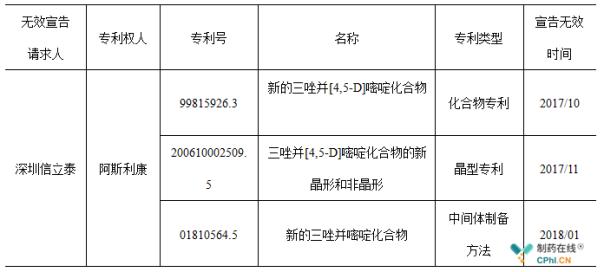
深圳信立泰替格瑞洛片化药4类仿制药上市申请于2017年3月9日获得CDE受理承办,是国内首家提交替格瑞洛片仿制药的制药企业。阿斯利康替格瑞洛化合物专利到期的时间为2019年12月2日,这是替格瑞洛的核心专利之一,信立泰通过专利挑战的方式先后突破了原研药物的化合物专利、晶型专利以及中间体制备方法专利,为旗下仿制药在国内的提前上市销售赢得了发展的空间。
在国内氯吡格雷的细分市场中,信立泰凭借泰嘉占据了大约30%的市场份额,同时泰嘉的主要规格产品75mg、25mg均已经首家通过了仿制药的一致性评价。此次,如果信立泰顺利拿下替格瑞洛片的国内首仿,那么公司将成为国内首个拥有氯吡格雷和替格瑞洛双品种的制药企业,这将大大提升公司在国内抗凝血药物领域的竞争力。
潜在重磅产品 国内仿制者众
自从上市以来,替格瑞洛的销售额增长较快,2016年的全球销售额为8.39亿美元。业内人士预测,替格瑞洛的销售额将在2019年超过氯吡格雷,成为抗凝血药物家族中新的引领者。
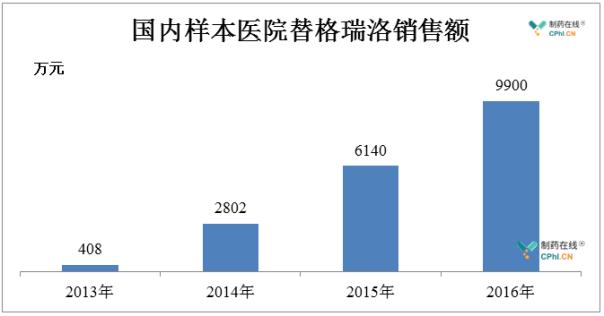
国内样本医院销售数据显示,2016年替格瑞洛销售额为9900万元,同比增长61.2%,是目前抗凝血药物中增速最为迅速的产品。2017年7月,替格瑞洛片被纳入到了国家医保谈判目录,最终价格下调22.8%进入医保,预计在国内市场中,替格瑞洛将形成对氯吡格雷市场份额的替代,销售实现快速增长。
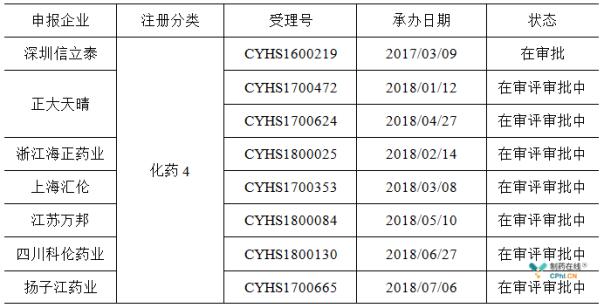
深圳信立泰替格瑞洛片化药4类仿制药上市申请于2017年11月被纳入到了CDE公布的第二十四批拟纳入优先审评程序药品注册申请的公示名单,历时7个月,信立泰的这款仿制药申请进入"在审批"状态,不得不说,这在很大程度上受益于优先审评程序的助力。
目前,国内以化药4类注册申报替格瑞洛片仿制药上市的制药企业共有7家,除了信立泰之外,包括正大天晴、浙江海正以及扬子江等在内的6家制药企业的7个受理号申请均处于状态"在审评审批中",CDE承办的日期处于2018年,进度明显落后于信立泰。