《自然-通讯》最新上线了一篇艾滋病研究领域的重磅论文。科学家们开发了一种联合疗法,将持续递送抗逆转录病毒的给药系统与CRISPR-Cas9基因编辑技术相配合。根据官方新闻稿,这种疗法首次从活体动物的基因组中消除了HIV-1的DNA。
研究机构评论说,这项研究“标志着在开发新疗法,治愈人类HIV感染的路上,迈出了关键一步”。
根据联合国艾滋病规划署(UNAIDS)的估计,全世界每一天新增的HIV-1病毒感染者超过5000人。目前,感染者主要依靠各种抗病毒药物进行治疗。抗逆转录病毒治疗(ART)能够有效降低患者体内的病毒载量,同时降低病毒传染的风险。
在科学家们的不懈努力下,现有疗法已经把曾经的绝症变成了可控的慢性疾病,而科学家们还在朝着治愈艾滋病的目标前进。
ART疗法要求感染者终生服药,因为这种疗法可以抑制HIV病毒的复制,却不能将病毒从体内消除。如果停药,体内的HIV病毒会卷土重来,重新复制并促进疾病发展。
而HIV之所以有“反弹”能力,是因为病毒在攻击人体的免疫系统时,会将DNA序列整合到细胞的基因组中,从而藏匿于人体。
要真正消除HIV达到“治愈”效果,就要从感染的细胞和组织中去除被病毒整合进去的DNA片段。
美国内布拉斯加大学医学中心(University of Nebraska Medical Center)的Howard Gendelman教授、坦普尔大学刘易斯·卡茨医学院(Lewis Katz School of Medicine at Temple University)的Kamel Khalili教授及同事开发了一种旨在消除HIV病毒的联合疗法,由一种ART递送新方法和CRISPR基因编辑技术组成。
具体来说,Gendelman教授及其合作者共同开发了一种长效缓释ART疗法,将结构经过改良的抗病毒药物分子包装在纳米颗粒中,由纳米颗粒将药物送入HIV的藏身之处。这种给药方式可以在数周内缓慢释放药物,达到在较长时间内抑制病毒活性的目的。
而Khalili教授团队利用CRISPR-Cas9开发的技术可以在受感染的细胞内“剪去”HIV的DNA片段。当长效缓释ART疗法将HIV病毒的复制抑制在较低水平的同时,CRISPR-Cas9开始发挥作用。
研究团队通过动物实验验证了这种联合疗法的可行性和有效性。他们首先制造了HIV感染的人源化小鼠模型。然后,分两次独立实验,给总计13只确认感染的小鼠施用了联合疗法。
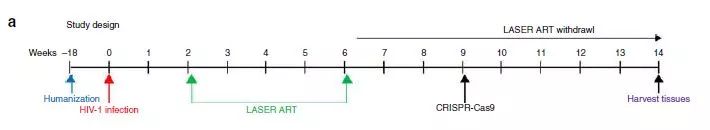
▲感染并施用疗法的研究示意图(图片来源:参考资料[1])
经过连续的治疗,接受治疗以后的5周内,通过多项技术对血液、淋巴组织、骨髓和脑组织进行检测。结果显示,接受联合疗法的小鼠中近三分之一没有检测到HIV病毒,可以被认为小鼠细胞和组织里的HIV病毒DNA被完全消除。
相比之下,单独接受其中某一种疗法的小鼠中,很容易就能检测到HIV。此外,检测结果还显示未检测到CRISPR-Cas9脱靶。
小鼠实验的积极结果显示了这种联合疗法治愈艾滋病的前景,据Khalili教授在研究机构发布的新闻中透露,他们计划开展进一步的研究,在一年内推进非人灵长类动物的试验,并有可能在人类患者身上展开临床试验。
参考资料
[1] Prasanta Dash et al., (2019) Sequential LASER ART and CRISPR Treatments Eliminate HIV-1 in a Subset of Infected Humanized Mice. Nature Communications. DOI: 10.1038/s41467-019-10366-y
