原创:Alice
2011年,ipilimumab治疗黑色素瘤适应症的批准标志着癌症免疫治疗(immuno-oncology)革命的开端,并且在近年来逐渐改变了癌症治疗的模式。自此之后,又有11个癌症免疫疗法被批准,很快成为多种癌症的标准疗法。为了解癌症免疫疗法的快速进展,2017年Cancer Research Institute发表了癌症免疫疗法的概况。近日,CRI的Jun Tang等学者在《Nature Reviews Drug Discovery》上再次发表了综述,就2018年免疫疗法的发展趋势做了详尽的分析。一年时间过去了,癌症免疫疗法发生了哪些变化呢?
全球癌症免疫疗法研发管线增长
在2017年9月至2018年9月这一年中,全球IO数量增长了67%(2017年2031个,2018年3394个)。具体分为6类:靶向T细胞的免疫调节剂(如PD-1或CTLA-4抗体);其他免疫调节剂(如Toll样受体TLR或IFNα/β受体IFNAR1激动剂);癌症疫苗(如BCG疫苗);细胞治疗(如嵌合抗原受体CAR或细胞受体TCR T细胞治疗);溶瘤病毒(如T-vec);靶向CD3的双特异性抗体(如blinatumomab)。这6类中细胞治疗的增长最大,为113%;溶瘤病毒药物数量增长最少,为16%;到2018年9月,细胞治疗已经超过癌症疫苗成为最大的IO药物种类,有864个,占所有IO类别的25%。另外,处于临床前阶段的数量增速高于临床阶段的(临床前从1067个增长到2107个,增长97%;临床阶段的从964个增长到1287个,增长34%)。

图1 全球IO研发管线变化趋势
(图片来源:Nat Rev Drug Discov. 2018 Oct 19. doi: 10.1038/nrd.2018.167)
癌症免疫疗法靶点增多
过去的一年,IO靶点数量增加50%,目前有417个。去年一半的研发集中在排名前23的靶点,今年一半集中在前48的靶点。已批准的药品靶点吸引力变小。如,虽然细胞治疗靶点增长113%,但CD19靶点增长只有37%。相反,新抗原(如从患者肿瘤中筛选的靶点)数量增加了113%。可见未来批准上市的靶点更趋多样化。值得注意的是,靶向非特异肿瘤相关抗原(tumour-associated antigens,TAA)的产品数量下降,说明研发瞄向更加精准的方向。

图2 2017年与2018年IO靶点数量对比
(图片来源:Nat Rev Drug Discov. 2018 Oct 19. doi: 10.1038/nrd.2018.167)
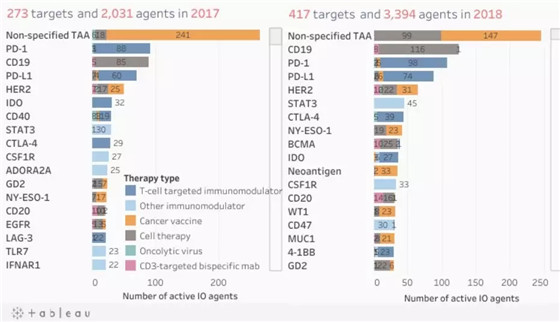
图3 2017年与2018年IO靶点前18位对比
(图片来源:http://www.cancerresearch.org/scientists/clinical-accelerator/landscape-of-immuno-oncology-drug-development)
更多机构参与癌症免疫疗法研发
2017年9月,有包括学术机构和产业界在内的总共461个机构在研发964个用于临床的药物。一年之后,有655个机构在研发1287个用于临床的药物,研发机构增加了42%,临床阶段的药物增加了34%。在排名前15的研发管线中,新增了36个,增加20%。大医药企业仍然占据主要位置,前15名中有4个新增的学术研究中心,其中三家来自中国,它们分别是深圳市免疫基因治疗研究院(Shenzhen Geno-Immune Medical Institute),中国人民解放军总医院(China PLA General Hospital),以及第三军医大学第一附属医院(Third Military Medical University Hospital One)。

(图片来源:Nat Rev Drug Discov. 2018 Oct 19. doi: 10.1038/nrd.2018.167)
结论
纵观一年来IO全球研发管线的变化,药物数量增加67%,药物靶点增加50%,临床阶段的药物研发机构增加了42%。巨量的增长说明IO药物研发领域热情饱满、前途光明。首先,2017年,FDA已批准了两个CAR T细胞治疗产品、8个PD-1和PD-L1抗体、1个靶向CD3的双特异性抗体。其次,新的免疫细胞治疗成为15种癌症的标准治疗,也成为黑色素瘤、肺癌、肾癌的前线治疗。再次,PD-1和PD-L1抗体等免疫治疗迅速进入美国以外的市场,如欧洲和日本。Nivolumab和pembrolizumab进入中国就是很好的例子。还有,免疫治疗的临床试验结果表明,其可以给患者带来长久的生存获益。这也给治愈癌症带来了希望。
然而,癌症免疫治疗基础研究向临床转化还需要十分谨慎。近期IDO1抑制剂的多个III期临床试验失败或终止再次提示了药物研发的高风险。扎实的基础研究是期进入临床的前提。例如,为筛选出最适合免疫疗法的患者需对生物标志物进行研究。另外,需要对大量临床试验进行综合分析,以吸收成功经验,学习失败教训,更好地指导今后的研究。
参考资料:
1.Nat Rev Drug Discov.2018 Oct 19. doi: 10.1038/nrd.2018.167
2.http://www.cancerresearch.org/scientists/clinical-accelerator/landscape-of-immuno-oncology-drug-development
