新一代抗雄激素药物如辉瑞(Pfizer)和安斯泰来(Astellas)的Xtandi,以及强生公司(Johnson & Johnson)的Zytiga,都能提高转移性去势抵抗性前列腺癌(mCRPC)的存活率。不过近期一支来自纽约大学的多学科研究团队合成了一种全新的化合物,有望进一步改善该疾病的治疗。
科学家一直在探索治疗前列腺癌的新方法,包括Wnt信号通路,这一通路在约20%的mCRPC病例中发生突变。Wnt激活会导致β连环蛋白的积累,它们与T细胞因子(TCF)转录因子结合,并触发促进细胞增殖的基因。这些基因的激活对于前列腺组织的早期发育至关重要,但它们也可能在成年期导致癌症。然而,针对该通路的药物发现仍然很不明确。
针对Wnt通路以及β连环蛋白和TCF的相互作用,纽约大学研究团队认为小分子并不适合蛋白质-蛋白质结合表面,因为这些表面通常是宽且平的,而由他们合成的这种新型化合物则非常适合。这种化合物介于小分子和大分子生物制剂之间,被称作拟肽。这些类蛋白质化合物具有与肽类似的结构,但在功能上却有显著差异。因为拟肽足够大,并且其结构能够抵抗蛋白质水解,所以有望成为靶向Wnt通路的新疗法。
关于该化合物的合成,研究人员解释道,他们将一个线性拟肽分子折叠成一个3D环状结构,并对其进行“装订”,使其刚好可以阻挡住TCF通常使用的对接部位。而新一代计算机模拟工具则使团队能够及早了解这种环状拟肽是如何适应其蛋白质目标的。
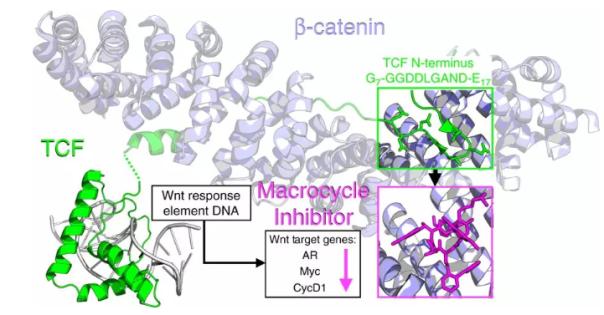
新型化合物靶向β连环蛋白与TCF相互作用的机制(图片来源:《Nature Communications》)
研究团队发现,在细胞培养实验中,与未经处理的细胞相比,这种环状拟肽在22天时能使前列腺癌细胞的生长减少95%。相比之下,用未经修饰的拟肽处理细胞,则仅能将癌细胞的生长减少40%。此外,它们还能减少雄激素的信号传导。研究人员认为,这表明它们可能具有双重抗癌作用。
研究团队希望在活体动物中证明这种新型化合物的作用,于是他们选择了斑马鱼。这些斑马鱼具有罕见的Wnt激活突变,会导致β连环蛋白积聚,阻止眼睛的形成。在实验中,研究人员发现,环状拟肽能阻断过度活跃的β连环蛋白与TCF相互作用,从而使斑马鱼发育出眼睛,这一相互作用类似于影响人类前列腺癌的相互作用。
这些结果让研究人员备受鼓舞,他们计划在前列腺癌小鼠模型中进一步测试这种化合物的治疗潜力。与此同时,他们认为β连环蛋白与TCF的相互作用也可能是治疗其他癌症类型(如结肠癌和乳腺癌)的良好靶点。
我们期待该研究团队能带来更多关于前列腺癌治疗的好消息,也期待有朝一日,人类可以攻克前列腺癌。
参考资料
[1] New 'peptoids' show promise in resistant prostate cancer. Retrieved Oct 26, 2018, from https://www.fiercebiotech.com/research/new-cyclic-peptoids-show-promise-resistant-prostate-cancer
[2] Jeffrey A. Schneider, et al., Design of Peptoid-peptide Macrocycles to Inhibit the β-catenin TCF Interaction in Prostate Cancer. Nature Communications, 2018, https://doi.org/10.1038/s41467-018-06845-3
