一位疫苗行业内部人士向南都记者分析称,“本次事件应该是内部举报,国家药监局有因检查,所以暂时仅涉及涉事批次。”
7月15日,国家药品监督管理局发布通告:国家药监局组织对长春长生生物科技有限责任公司(以下简称“长春长生”)开展飞行检查,发现长春长生在冻干人用狂犬病疫苗生产过程中存在记录造假等严重违反《药品生产质量管理规范》(药品GMP)行为。国家药监局迅速责成吉林省食品药品监督管理局收回长春长生相关《药品GMP证书》,即不允许继续生产狂苗。
① 什么是“生产过程中存在记录造假”?
《药品生产质量管理规范》(GMP)规定,每批药品应当有批记录,包括批生产记录、批包装记录、批检验记录和药品放行审核记录等与本批产品有关的记录。批记录应当由质量管理部门负责管理,至少保存至药品有效期后一年。
国家药监局通报,此次问题是“在冻干人用狂犬病疫苗生产过程中存在记录造假”。
GMP规定明确,生产管理负责人的主要职责中,包括“确保批生产记录和批包装记录经过指定人员审核并送交质量管理部门”。
什么是生产记录?每批产品均应当有相应的批生产记录,可追溯该批产品的生产历史以及与质量有关的情况。
GMP规定,在生产过程中,生产者在进行每项操作时应当及时记录,操作结束后,应当由生产操作人员确认并签注姓名和日期。
这些需要记录的操作项目包括:产品名称、规格、批号;生产以及中间工序开始、结束的日期和时间;每一生产工序的负责人签名;必要时,还应当有操作(如称量)复核人员的签名;每一原辅料的批号以及实际称量的数量(包括投入的回收或返工处理产品的批号及数量);相关生产操作或活动、工艺参数及控制范围,以及所用主要生产设备的编号;中间控制结果的记录以及操作人员的签名;不同生产工序所得产量及必要时的物料平衡计算以及对特殊问题或异常事件的记录,包括对偏离工艺规程的偏差情况的详细说明或调查报告等。
目前,尚不清楚记录造假是在产品生产的什么环节。
药品管理法明确,除中药饮片的炮制外,药品必须按照国家药品标准和国务院药品监督管理部门批准的生产工艺进行生产,生产记录必须完整准确。药品生产企业改变影响药品质量的生产工艺的,必须报原批准部门审核批准。
② 生产过程中,为何会出现“记录造假”?
“现在冻干人用狂犬病疫苗生产存在记录造假具体原因还不知道,等待相关部门调查结果。”长生生物董秘赵春志回应媒体称。
对此,一位疫苗行业内部人士向南都记者分析称,“本次事件应该是内部举报,国家药监局有因检查,所以暂时仅涉及涉事批次。”
疫苗专家陶黎纳撰文指出,“狂犬病疫苗的生产成本中,疫苗有效成分的成本是最高的,所以厂家才会想出用佐剂来减量增效,降低成本。另一方面,狂苗的有效成分检测可能也存在一定的难度,厂家选择铤而走险。”
前述内部人士说,狂犬疫苗确实是生产控制非常难的疫苗,检定也很难,现在的批签发监管非常严格,企业作假的目的应该是为了能通过批签发检验。
按照批签发的流程,企业完成生产首先要在企业内部做出厂检验,企业自检合格之后,企业提出疫苗批签发申请,各个省级药监局会在5个工作日内组织抽样,将样品封存,随后由企业送到中检院或其他授权进行批签发的省级药检机构。
除了疫苗的样品,企业同时还要提交该批次的生产和检验记录摘要文件。之后,疫苗样品会被分派给各个检验人员,做不同的检验项目。
同时,还有一部分人负责对企业提交的批生产和检验记录摘要做逐一审核,这些文件记录了疫苗产品生产和企业自检的最关键的步骤和数据。
“批签发过程中,检验只是一部分,资料审核也是非常重要的。”中检院生物制品检定所一名专家此前接受南都采访时说。
③ 生产记录造假,疫苗质量是否有问题?
前述内部人士透露,涉事批次在产品质量和疫苗效价上是否存在问题,“目前正在检验中”。
根据中国疫苗上市有关规定,所有疫苗产品,无论是进口还是国产,都需要经过批签发程序才能上市。
据南都记者了解,批签发过程中的检验的项目包括疫苗体内外的效力、安全性、理化检验等等。效力评价是看疫苗能否激发免疫反应;理化检验则包括疫苗的纯度、pH值、渗透压等等。
疫苗是一种生物制品,它的效力评价往往会用到动物实验,比如将疫苗接种到小鼠身上,然后再将过量的致病性的微生物注入小鼠体内,评估经免疫的实验动物的疫苗保护作用。这个过程大致是模拟人体接种疫苗后受到病原微生物感染的过程,从而得出对疫苗效力的评价。
前述内部人士介绍,狂犬疫苗的有效性检查也是通过动物实验完成的,这是世界卫生组织WHO订立的金标准方法,主要是评价疫苗的保护力,方法跟百白破疫苗是相似的。他表示,“狂犬疫苗确实是生产控制非常难的疫苗,检定也很难。”
此次狂犬疫苗门事件曝光后,长春长生发布公告称,为了保证用药安全,公司正对有效期内所有批次的冻干人用狂犬病疫苗(Vero细胞)全部实施召回。根据长春长生近几年对该疫苗不良反应监测,未发现因产品质量问题引起的不良反应。
④ 近几年,对狂犬疫苗的质控如何?
根据《2017年生物制品批签发年报》,2017年在对人用狂犬病疫苗进行批签发检验中,7批疫苗不符合规定。其中1批为国产,6批为进口。
其中广州诺诚生物制品股份有限公司生产的1批冻干人用狂犬病疫苗(Vero细胞)和凯荣-贝林公司(境外企业)生产的2批人用狂犬病疫苗(鸡胚细胞)的效力试验不符合规定;凯荣-贝林公司生产的4批人用狂犬病疫苗(鸡胚细胞)的细菌内毒素和热原检查项不符合规定。
在批签发发现问题后,国家药监局启动对凯荣-贝林公司生产的人用狂犬病疫苗(鸡胚细胞)的市场专项抽验,即对已经签发上市的疫苗进行市场监督抽验,检验结果均符合规定。
“这说明批签发能够有效阻止不合格产品流入市场。”《2017年生物制品批签发年报》称。
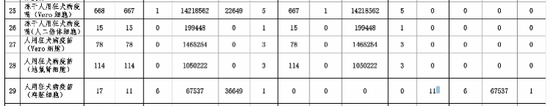
2017年批签发中通过和拒绝的疫苗产品。来源:《2017年生物制品批签发年报》
⑤ 如何评估此次事件对公共安全的影响?
国家药监局的公告中表示,“此次飞行检查所有涉事批次产品,尚未出厂和上市销售,全部产品已得到有效控制。”
南都记者注意到,事件经国家药监局曝光后,多地也对外表示,目前该批次产品尚未对外出售。广东省疾控中心表示,目前,这次飞行检查所有涉事批次产品尚未出厂和上市销售,全部产品已得到有效控制。因此,广东省没有涉事批次疫苗。目前并未发现接种狂犬疫苗后不良反应发生率异常的情况。
其他批次的疫苗有无问题?
除了已经停产的部分外,长生生物称:“为了保证用药安全,长春长生正对有效期内所有批次的冻干人用狂犬病疫苗(vero细胞)全部实施召回。”
根据公开资料显示,2017年长生生物将近99%的收入来自疫苗,其中冻干人用狂犬疫苗(Vero细胞)是子公司长春长生的核心产品之一,狂犬病疫苗在2017年的批签发数量达到355万人份,位居国内第二位。
⑥ 事件曝光后续将如何处置?
目前,国家药监局已要求吉林省食品药品监督管理局收回该企业《药品GMP证书》,责令停止狂犬疫苗的生产,责成企业严格落实主体责任,全面排查风险隐患,主动采取控制措施,确保公众用药安全。
吉林省食品药品监督管理局调查组已进驻该企业,对相关违法违规行为立案调查。国家药品监督管理局派出专项督查组,赴吉林督办调查处置工作。
国家药监局也表示,对发现的违法违规问题绝不姑息,坚决依法依规严肃查处,涉嫌构成犯罪的,一律移送公安机关予以严惩。
不过,目前,还不清楚事情的性质严重到何种程度。
在此之前,2008年大连金港安迪公司在生产狂苗时,在疫苗中添加了增强效果的佐剂——核酸。添加核酸可以让狂苗在有效成分低于国家标准的情况下,实际免疫效果等同于合格疫苗,为企业降低1/3甚至一半以上的生产成本。
也就是说,原来只能生产1支疫苗的原料,现在可以用来生产2支。然而,核酸作为佐剂用于人用疫苗,并未被我国批准过。
根据药品管理法,药品的生产企业未按照规定实施《药品生产质量管理规范》的,给予警告,责令限期改正;逾期不改正的,责令停产、停业整顿,并处五千元以上二万元以下的罚款;情节严重的,吊销《药品生产许可证》。
2009年,大连金港安迪公司为自己的行为付出严重代价。国家药监局注销大连金港安迪生物制品有限公司药品批准文号和《药品GMP证书》,并依法吊销其《药品生产许可证》。
⑦ 狂犬病在我国的疾病负担如何?
根据国家卫健委网站介绍,狂犬病是一种病毒性疾病,主要是通过咬伤传播,但也可以通过破损的皮肤或粘膜污染被感染动物的唾液而传播,引起的人兽共患的中枢神经系统传染病,多见于犬、猫等动物,病死率高达100%。
20世纪50年代以来,我国人间狂犬病先后出现过3次流行高峰,分别是在20世纪50年代中期,20世纪80年代初期和21世纪初。
进入21世纪后,狂犬病仍然是重要的公共卫生威胁,全球每年约有60000人死于狂犬病,是致死人数最多的动物源性传染病,每年由此引发的经济负担约为40亿美元。中国人间狂犬病发病仅次于印度,2007年疫情高峰时,年报告病例数达3300例。2004-2014?年,狂犬病死亡人数一直高居我国传染病死亡数的前3位。此外,调查显示,部分地区狂犬病漏报率可能高达35%,这提示我国狂犬病的疾病负担可能存在低估。
在第三次疫情高峰前后,我国采取了一系列遏制狂犬病的措施,包括落实人间狂犬病防控措施、建立狂犬病多部门防控机制、强化犬只管理和动物狂犬病防治,以及加强人用狂犬病疫苗和被动免疫制剂质量监管等,取得了较为显著的防治效果。自2008年起,我国狂犬病疫情出现持续回落,至2014年报告发病数已降至1000例以下,较2007年的峰值下降了72%。
