今日,《自然》子刊《自然·纳米技术》(Nature Nanotechnology)在线刊登了一项创新抗癌研究:加州大学洛杉矶分校(UCLA)华人学者顾臻教授与其团队开发出了一种新型癌症免疫治疗策略。通过在肿瘤切除部位喷洒喷雾,快速形成凝胶,并通过包埋其中的纳米颗粒缓释抗体药物,研究人员在动物模型上验证了该种喷剂能靶向手术后的残余癌细胞,显著抑制癌症复发和潜在的转移。
对于不少癌症患者来说,肿瘤切除手术是必要且有效的治疗方法。例如,被诊断为乳腺癌早期的患者,有95%需要进行手术;而对于脑肿瘤患者来说,手术更是一线治疗方法。然而,尽管近些年来手术技术得到不断改善,术后难免存在残余的癌细胞,有些癌细胞甚至还会进入外周血液循环。因此,接受手术治疗的患者,术后复发常有发生。而据统计,大约九成癌症患者最后是因为肿瘤复发或癌症转移而死亡。
那么,有什么办法能够在术后最大程度防止肿瘤卷土重来,同时没有明显的毒副作用呢?这正是顾臻教授团队想要回答的问题。
首先,研究人员们指出,免疫系统之所以难把癌细胞赶尽杀绝,一大原因在于癌细胞的“表面功夫”太厉害——在很多癌细胞表面,都高水平表达一种叫作CD47的分子。这种整合素相关蛋白令癌细胞仿佛贴上免死金牌,向巨噬细胞打出“别吃我”的信号,从而逃过一死。好在自从癌细胞的这套策反攻略被科学家揭发以后,人们已经找到几种可以阻断CD47的特异性抗体,也让CD47成为富有潜力的癌症治疗靶点。顾臻教授的研究团队就是利用这类抗体来对付术后肿瘤余孽,让免疫系统认清它们的真面目,将之清除。
但是,CD47并非癌细胞的专属。事实上,人体内数量最多、新旧更替最快的一类细胞——红细胞表面,CD47就起了重要的作用。它能保证衰老红细胞被免疫系统清除、同时年轻红细胞不被误伤。因此,如果全身用药阻断CD47,杀敌的同时就容易自损,有引起贫血等问题的风险。
为了把药物较精准地递送到肿瘤切除部位,致力于开发新型药物递送系统的顾臻团队设计了一种精巧的方式。他们先把这些抗体装进纳米颗粒中,再采用喷雾的形式,局部施加到手术部位。
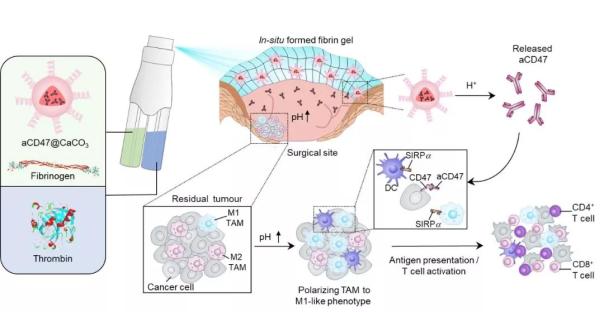
通过一个双储液喷雾器,喷雾溶液中的纤维蛋白原和凝血酶一经混合,会迅速在伤口处形成凝胶状的纤维蛋白,有助于止血并促进伤口愈合。与此同时,喷雾里的纳米颗粒也会一步到位凝固在凝胶内,直接作用于伤口。研究人员们制造的这些纳米颗粒,所选用的材料是碳酸钙。在呈现微酸性的伤口及肿瘤微环境里,这些颗粒可以被逐渐溶解,释放其中的抗CD47药物。
▲喷雾凝胶示意图:包埋在纤维蛋白胶里的碳酸钙纳米颗粒缓释出的抗体可以封闭癌细胞表面表达的CD47(图片来源:参考资料[1])
此外,这种纳米颗粒载体本身还能带来一定的治疗优势。当伤口及潜在肿瘤微酸环境被碳酸钙“中和”后,“还可以增强巨噬细胞的活性,加强它们清除体内异物的能力。”论文第一作者陈倩博士说。
研究人员通过动物实验测试了这种喷雾凝胶的效果。在接受了手术切除的晚期黑色素瘤小鼠中,术后用凝胶做了处理的小鼠,有半数没有再检测到残余的肿瘤细胞。这显著提高了对肿瘤再生的控制,这些小鼠的术后生存时间也至少达到60天。
有意思的是,这种喷雾凝胶不仅在切除肿瘤的部位严防死守,抑制复发,还能抑制肿瘤在体内其他部位的发展。顾臻教授介绍说,在模拟癌症转移的小鼠中,手术局部施加喷雾凝胶后,远端的肿瘤生长也得到了抑制。“我们发现免疫系统中的T细胞也会被这种治疗性凝胶激活,一起调动起来,攻击潜在的癌细胞。”陈倩博士补充道。
▲在癌症转移的小鼠模型中,在手术切除部位(右侧)用凝胶处理后,远端的肿瘤(左侧)生长也得到了控制(图片来源:参考资料[1])
下一步,研究团队将继续通过动物实验摸索这种喷剂的最佳剂量、纳米颗粒的最佳组合和理想的施加频率等,为潜在应用于临床做好准备。
我们祝贺顾臻教授团队的这项癌症免疫治疗策略在动物模型中得到验证,也期待这种抗癌喷雾凝胶进一步发挥潜能,帮助扫清治愈癌症道路上的障碍。
参考资料
[1] Qian Chen et al., (2018), In situ sprayed bioresponsive immunotherapeutic gel for post-surgical cancer treatment, Nature nanotechnology, DOI: 10.1038/s41565-018-0319-4
