作者: 王晓晴
2017年至今(截止到12.26日)CDE总共公布了13批拟纳入优先审评程序药品注册申请的公示,合计219件(以受理号计)。
国产申报125件中,仿制药几乎是新药申请的两倍,且均为仿制药上市申请。进口申报94件中,新药申请占95%,其中,临床和上市申请几乎各占一半。
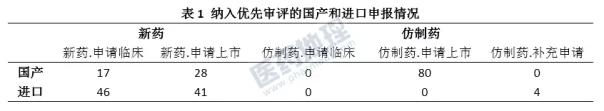
化药共计184件,与生物制品和中药相比占据绝对优势,其中仅化药上市申请达134件之多。中药临床申请仅2件,均以儿童用药品作为入选理由。
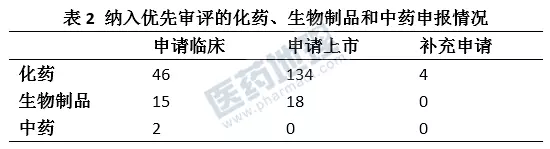
以通用名计,总共113个品种,其中Palbociclib(帕布昔利布)涉及的受理号最多,为6个,是辉瑞申报的靶向小分子抗肿瘤药,因与现有治疗手段相比具有明显治疗优势纳入优先审评。
1、江苏恒瑞入选品种最多
以通用名计,江苏恒瑞优先审评品种数目最多,为7个,其次为浙江华海的5个。正大天晴、连云港润众、广东东阳光和GSK品种数排名并列第三,均为4个品种。
江苏恒瑞作为本土药企中的“研发一哥”取得这样的成绩并不奇怪,7个品种中有3个为抗肿瘤药,其中,吡咯替尼为EGFR/HER2靶向抑制剂,作为1类新药申报,用于治疗HER2阳性转移性乳腺癌。浙江华海均为仿制药纳入。

2、11个品种多家企业纳入
苯达莫司汀涉及企业最多,为4家,除泰卫医药外均为国内企业,南京先声东元制药和正大天晴分别以“治疗慢性淋巴细胞白血病(CLL)首家申请”和“治疗非霍奇金淋巴瘤(NHL)首家申请”为由纳入优先审评。
因有多家企业隶属于同一集团或者为子母公司关系,去除这些因素,真正同一品种有2家以上企业纳入的,除了苯达莫司汀外,还有莫西沙星、阿齐沙坦和紫杉醇(白蛋白结合型),且均为上市申请。

3、靶向小分子抗肿瘤药抢眼
从治疗分类看,抗肿瘤药纳入件数最多,为46件,占了五分之一。其次为抗感染药和内分泌及代谢调节用药。
而从治疗小类来看,仅靶向小分子药物就有27件之多,涉及国外企业如辉瑞、武田,国内企业如恒瑞、正大天晴、和记黄埔等。其次为抗肝炎病毒药为13件和抗抑郁药12件。

4、“具有明显治疗优势”成为本年度最多入选理由
从入选理由来看,“与现有治疗手段相比具有明显治疗优势”入选数量最多,其次为“同一生产线生产,已在美国/欧盟上市”和“儿童用药品”。
当然也有少数品种以多个理由入选,如表7,这两个品种均有3个入选理由。LCAR-B38MCAR-T细胞自体回输制剂是我国首个申请临床的CAR-T类药物。注射用盐酸美法仑用于治疗罕见病多发性骨髓瘤,其进入优先审评通道,有助于日后弥补我国美法仑市场的空白。

(本文数据均来源于:中国医药工业信息中心CPM数据库)
